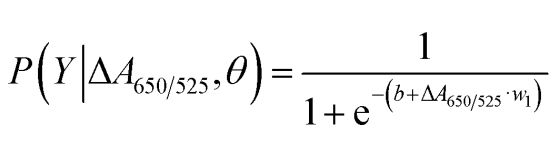Die Früherkennung von Krebs mittels Flüssigbiopsie ist ein neuer Ansatz in der Krebsdiagnostik, der in den letzten Jahren vom US-amerikanischen National Cancer Institute (NCI) entwickelt wurde. Ziel ist die Erkennung von Krebs im Frühstadium oder sogar von Krebsvorstufen. Flüssigbiopsien werden bereits häufig als neuartiger Biomarker für die Früherkennung verschiedener maligner Erkrankungen eingesetzt, darunter Lungenkrebs, gastrointestinale Tumoren, Gliome und gynäkologische Tumoren.
Die Entwicklung von Plattformen zur Identifizierung von Methylierungslandschafts-Biomarkern (Methylscape) birgt das Potenzial, die bestehenden Früherkennungsmethoden für Krebs deutlich zu verbessern und Patienten in das frühestmögliche behandelbare Stadium zu bringen.
Forscher haben kürzlich eine einfache und direkte Sensorplattform zur Detektion des Methylierungsmusters entwickelt. Diese basiert auf mit Cysteamin dekorierten Goldnanopartikeln (Cyst/AuNPs) und einem Smartphone-basierten Biosensor, der ein schnelles Früherkennungsscreening verschiedenster Tumore ermöglicht. So kann beispielsweise innerhalb von 15 Minuten nach DNA-Extraktion aus einer Blutprobe ein Früherkennungsscreening von Leukämie mit einer Genauigkeit von 90 % durchgeführt werden. Der Titel des Artikels lautet: „Schneller Nachweis von Krebs-DNA im menschlichen Blut mithilfe von mit Cysteamin beschichteten AuNPs und einem Smartphone mit maschinellem Lernen“.
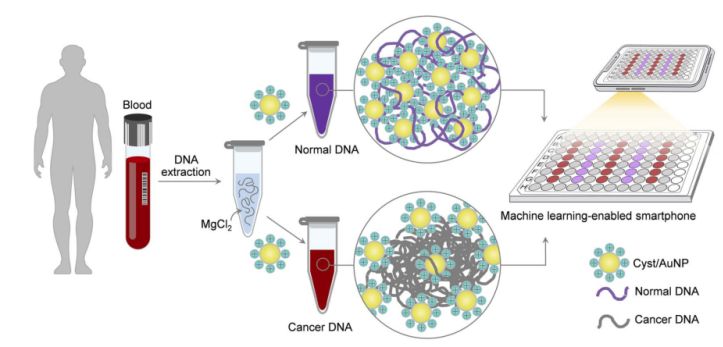
Abbildung 1. Eine einfache und schnelle Sensorplattform für das Krebs-Screening mittels Cyst/AuNPs-Komponenten kann in zwei einfachen Schritten realisiert werden.
Dies ist in Abbildung 1 dargestellt. Zunächst wurden die DNA-Fragmente in einer wässrigen Lösung gelöst. Anschließend wurden Cyst/AuNPs zu der Lösung hinzugefügt. Normale und maligne DNA weisen unterschiedliche Methylierungseigenschaften auf, was zu DNA-Fragmenten mit unterschiedlichen Selbstassemblierungsmustern führt. Normale DNA aggregiert locker und aggregiert schließlich auch Cyst/AuNPs, was zu einer Rotverschiebung der Cyst/AuNPs führt. Der Farbumschlag von Rot nach Violett ist mit bloßem Auge sichtbar. Im Gegensatz dazu führt das spezifische Methylierungsprofil von Krebs-DNA zur Bildung größerer Cluster von DNA-Fragmenten.
Die Bilder der 96-Well-Platten wurden mit einer Smartphone-Kamera aufgenommen. Die Krebs-DNA wurde mittels eines mit maschinellem Lernen ausgestatteten Smartphones im Vergleich zu spektroskopischen Methoden gemessen.
Krebsvorsorge anhand realer Blutproben
Um die Anwendbarkeit der Sensorplattform zu erweitern, setzten die Forscher einen Sensor ein, der erfolgreich zwischen normaler und krebsartiger DNA in realen Blutproben unterscheiden konnte. Methylierungsmuster an CpG-Stellen regulieren die Genexpression epigenetisch. Bei nahezu allen Krebsarten wurden alternierende Veränderungen der DNA-Methylierung und damit der Expression von Genen beobachtet, die die Tumorentstehung fördern.
Als Modell für andere Krebsarten, die mit DNA-Methylierung in Zusammenhang stehen, nutzten die Forscher Blutproben von Leukämiepatienten und gesunden Kontrollpersonen, um die Aussagekraft des Methylierungsprofils bei der Differenzierung von Leukämie-Tumoren zu untersuchen. Dieser Biomarker des Methylierungsprofils übertrifft nicht nur bestehende Schnelltests zur Leukämie-Diagnostik, sondern zeigt auch, dass er sich mit diesem einfachen und unkomplizierten Testverfahren auf die Früherkennung einer Vielzahl von Krebsarten ausweiten lässt.
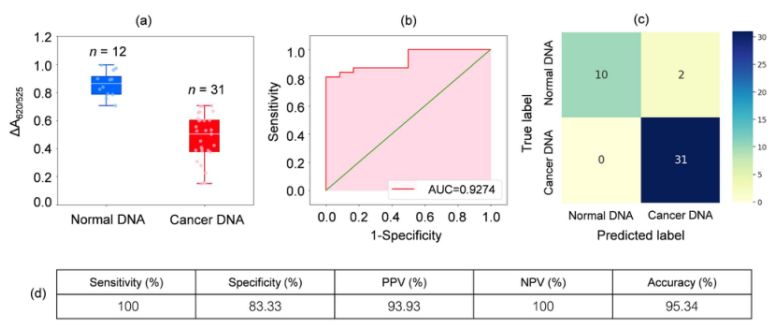
DNA aus Blutproben von 31 Leukämiepatienten und 12 gesunden Probanden wurde analysiert. Wie im Boxplot in Abbildung 2a dargestellt, war die relative Absorption der Krebsgewebeproben (ΔA650/525) geringer als die der DNA aus den Kontrollproben. Dies war hauptsächlich auf die erhöhte Hydrophobizität zurückzuführen, die zu einer dichten Aggregation der Krebs-DNA führte und die Aggregation der Cyst/AuNPs verhinderte. Dadurch waren diese Nanopartikel vollständig in den äußeren Schichten der Krebsaggregate dispergiert, was zu einer unterschiedlichen Dispersion der an normale und Krebs-DNA-Aggregate adsorbierten Cyst/AuNPs führte. Anschließend wurden ROC-Kurven erstellt, indem der Schwellenwert von einem Minimalwert von ΔA650/525 bis zu einem Maximalwert variiert wurde.
Abbildung 2.(a) Relative Absorptionswerte von Zysten/AuNP-Lösungen, die das Vorhandensein normaler (blau) und Krebs-DNA (rot) unter optimierten Bedingungen zeigen.
(DA650/525) Boxplots; (b) ROC-Analyse und Bewertung diagnostischer Tests. (c) Konfusionsmatrix zur Diagnose von gesunden und an Krebs erkrankten Patienten. (d) Sensitivität, Spezifität, positiver prädiktiver Wert (PPV), negativer prädiktiver Wert (NPV) und Genauigkeit der entwickelten Methode.
Wie in Abbildung 2b dargestellt, zeigte die Fläche unter der ROC-Kurve (AUC = 0,9274) des entwickelten Sensors eine hohe Sensitivität und Spezifität. Aus dem Boxplot geht hervor, dass der niedrigste Punkt (normale DNA) nicht deutlich vom höchsten Punkt (Krebs-DNA) getrennt ist. Daher wurde eine logistische Regression verwendet, um zwischen den Gruppen zu differenzieren. Diese schätzt anhand unabhängiger Variablen die Wahrscheinlichkeit des Eintretens eines Ereignisses (Krebs oder normales Gewebe). Die abhängige Variable liegt zwischen 0 und 1. Das Ergebnis ist somit eine Wahrscheinlichkeit. Die Wahrscheinlichkeit der Krebsidentifizierung (P) wurde anhand von ΔA650/525 wie folgt bestimmt.
wobei b = 5,3533 und w1 = -6,965. Bei der Probenklassifizierung deutet eine Wahrscheinlichkeit unter 0,5 auf eine normale Probe hin, während eine Wahrscheinlichkeit von 0,5 oder höher auf eine Krebsprobe hinweist. Abbildung 2c zeigt die Konfusionsmatrix der Leave-it-alone-Kreuzvalidierung, die zur Validierung der Stabilität des Klassifizierungsverfahrens verwendet wurde. Abbildung 2d fasst die Ergebnisse der diagnostischen Testbewertung des Verfahrens zusammen, einschließlich Sensitivität, Spezifität, positivem prädiktivem Wert (PPV) und negativem prädiktivem Wert (NPV).
Smartphone-basierte Biosensoren
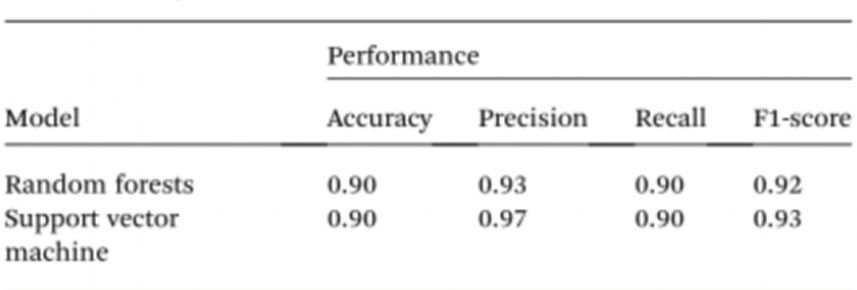
Um die Probenanalyse ohne Spektrophotometer weiter zu vereinfachen, nutzten die Forscher künstliche Intelligenz (KI), um die Farbe der Lösung zu interpretieren und zwischen gesunden und krebskranken Personen zu unterscheiden. Dazu wurde Computer Vision eingesetzt, um die Farbe der Cyst/AuNPs-Lösung anhand von Bildern aus 96-Well-Platten, die mit einer Handykamera aufgenommen wurden, in normale DNA (lila) oder krebsartige DNA (rot) umzuwandeln. Künstliche Intelligenz kann die Kosten senken und die Zugänglichkeit der Farbinterpretation von Nanopartikellösungen verbessern, ohne dass optische Hardware oder Smartphone-Zubehör benötigt wird. Abschließend wurden zwei Modelle des maschinellen Lernens, Random Forest (RF) und Support Vector Machine (SVM), trainiert, um die Modelle zu erstellen. Beide Modelle klassifizierten die Proben mit einer Genauigkeit von 90,0 % korrekt als positiv oder negativ. Dies deutet darauf hin, dass der Einsatz von künstlicher Intelligenz in der mobiltelefonbasierten Biosensorik durchaus machbar ist.
Abbildung 3. (a) Zielklasse der Lösung, aufgezeichnet während der Probenvorbereitung für die Bildaufnahme. (b) Beispielbild, aufgenommen während der Bildaufnahme. (c) Farbintensität der Zysten/AuNP-Lösung in den einzelnen Vertiefungen der 96-Well-Platte, extrahiert aus Bild (b).
Mithilfe von Cyst/AuNPs haben Forscher erfolgreich eine einfache Sensorplattform zur Detektion des Methylierungsmusters und einen Sensor entwickelt, der in der Lage ist, normale DNA von Krebs-DNA in realen Blutproben für das Leukämie-Screening zu unterscheiden. Der entwickelte Sensor demonstrierte, dass aus realen Blutproben extrahierte DNA geringe Mengen an Krebs-DNA (3 nM) bei Leukämiepatienten innerhalb von 15 Minuten schnell und kostengünstig nachweisen konnte und eine Genauigkeit von 95,3 % erreichte. Um die Probenanalyse weiter zu vereinfachen und den Einsatz eines Spektralphotometers überflüssig zu machen, wurde maschinelles Lernen eingesetzt, um die Farbe der Lösung zu interpretieren und anhand eines Handyfotos zwischen gesunden und an Krebs erkrankten Personen zu unterscheiden. Auch hier wurde eine Genauigkeit von 90,0 % erzielt.
Referenz: DOI: 10.1039/d2ra05725e
Veröffentlichungsdatum: 18. Februar 2023
 中文网站
中文网站