Nat Med | Ein Multi-Omics-Ansatz zur Kartierung der integrierten Tumor-, Immun- und Mikrobenlandschaft von Darmkrebs enthüllt die Wechselwirkung des Mikrobioms mit dem Immunsystem
Obwohl Biomarker für primären Darmkrebs in den letzten Jahren intensiv erforscht wurden, stützen sich die aktuellen klinischen Leitlinien zur Festlegung von Behandlungsempfehlungen lediglich auf das Tumor-Lymphknoten-Metastasen-Stadium und den Nachweis von DNA-Mismatch-Reparaturdefekten (MMR) oder Mikrosatelliteninstabilität (MSI) (zusätzlich zu Standard-Pathologieuntersuchungen). Forscher haben in der Kohorte des Cancer Genome Atlas (TCGA) für Darmkrebs festgestellt, dass kein Zusammenhang zwischen Genexpressions-basierten Immunantworten, mikrobiellen Profilen und Tumorstroma einerseits und dem Patientenüberleben andererseits besteht.
Im Zuge der Forschung wurde festgestellt, dass quantitative Merkmale des primären kolorektalen Karzinoms, einschließlich der zellulären, immunologischen, stromalen oder mikrobiellen Natur des Tumors, signifikant mit den klinischen Ergebnissen korrelieren. Allerdings ist das Verständnis darüber, wie sich ihre Wechselwirkungen auf die Patientenergebnisse auswirken, noch immer begrenzt.
Um den Zusammenhang zwischen phänotypischer Komplexität und Krankheitsverlauf zu untersuchen, entwickelte und validierte ein Forscherteam des Sidra Institute of Medical Research in Katar kürzlich einen integrierten Score (mICRoScore). Dieser identifiziert Patienten mit guten Überlebensraten durch die Kombination von Mikrobiom-Charakteristika und Immunabstoßungskonstanten (ICR). Das Team führte eine umfassende Genomanalyse von frisch gefrorenen Proben von 348 Patienten mit primärem Kolorektalkarzinom durch. Diese umfasste die RNA-Sequenzierung von Tumoren und zugehörigem gesundem Kolorektalgewebe, die Exomsequenzierung, die Sequenzierung des T-Zell-Rezeptors und des bakteriellen 16S-rRNA-Gens sowie die Sequenzierung des gesamten Tumorgenoms zur weiteren Charakterisierung des Mikrobioms. Die Studie wurde in Nature Medicine unter dem Titel „An integrated tumor, immune and microbiome atlas of colon cancer“ veröffentlicht.

Der Artikel wurde in Nature Medicine veröffentlicht.
AC-ICAM-Übersicht
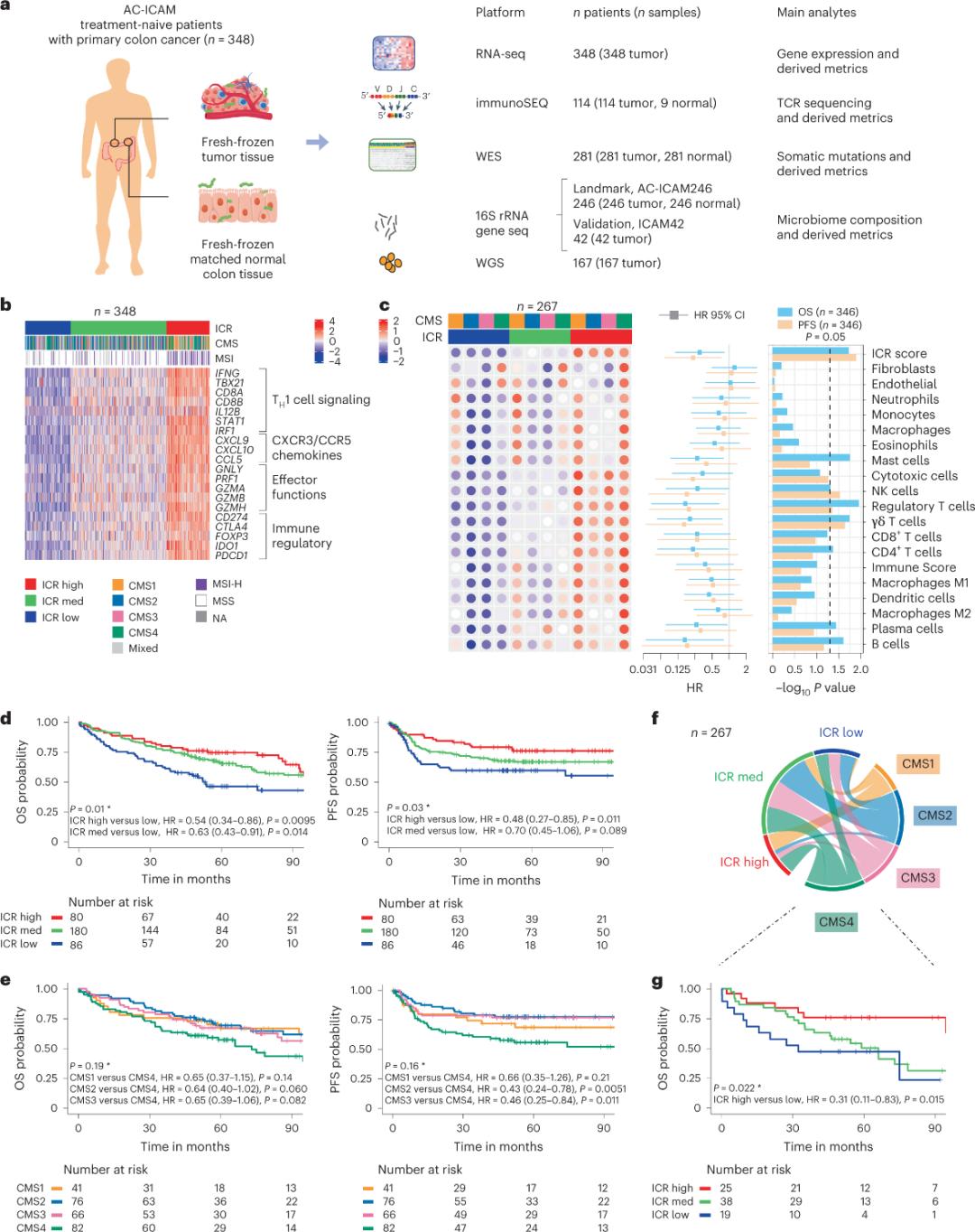
Forscher nutzten eine orthogonale Genomplattform, um frisch gefrorene Tumorproben und zugehöriges gesundes Kolongewebe (Tumor-Normalgewebe-Paare) von Patienten mit histologisch gesichertem Kolonkarzinom ohne systemische Therapie zu analysieren. Basierend auf der Exomsequenzierung (WES), der Qualitätskontrolle der RNA-Seq-Daten und der Überprüfung der Einschlusskriterien wurden Genomdaten von 348 Patienten für die nachfolgende Analyse mit einer medianen Nachbeobachtungszeit von 4,6 Jahren ausgewählt. Das Forschungsteam nannte diese Ressource Sidra-LUMC AC-ICAM: Eine Karte und ein Leitfaden zu den Wechselwirkungen zwischen Immunsystem, Krebs und Mikrobiom (Abbildung 1).
Molekulare Klassifizierung mittels ICR
Das Forschungsteam erfasste einen modularen Satz immunologischer Marker zur kontinuierlichen Immunüberwachung von Krebs, die sogenannte Immunkonstante der Abstoßung (ICR), und optimierte diese, indem es sie in ein Panel aus 20 Genen komprimierte, das verschiedene Krebsarten wie Melanom, Blasenkrebs und Brustkrebs abdeckt. Die ICR wurde auch mit dem Ansprechen auf Immuntherapien bei verschiedenen Krebsarten, einschließlich Brustkrebs, in Verbindung gebracht.
Zunächst validierten die Forscher die ICR-Signatur der AC-ICAM-Kohorte mithilfe eines ICR-Gen-basierten Co-Klassifizierungsansatzes, um die Kohorte in drei Cluster/immunologische Subtypen einzuteilen: hohe ICR (heiße Tumoren), mittlere ICR und niedrige ICR (kalte Tumoren) (Abbildung 1b). Die Forscher charakterisierten die mit den Konsensus-Molekularsubtypen (CMS) assoziierte Immunneigung. CMS ist eine Transkriptom-basierte Klassifizierung von Darmkrebs. Die CMS-Kategorien umfassen CMS1/immunologisch, CMS2/kanonisch, CMS3/metabolisch und CMS4/mesenchymal. Die Analyse zeigte, dass die ICR-Werte in allen CMS-Subtypen negativ mit bestimmten Signalwegen der Krebszellen korrelierten. Positive Korrelationen mit immunsuppressiven und stromabezogenen Signalwegen wurden nur in CMS4-Tumoren beobachtet.
In allen CMS war die Häufigkeit von natürlichen Killerzellen (NK-Zellen) und T-Zell-Subpopulationen in den ICR-hohen Immunsubtypen am höchsten, während andere Leukozyten-Subpopulationen eine größere Variabilität aufwiesen (Abbildung 1c). Die ICR-Immunsubtypen zeigten unterschiedliche Gesamtüberlebens- (OS) und progressionsfreie Überlebenszeiten (PFS), wobei der ICR-Wert von niedrig zu hoch progressiv anstieg (Abbildung 1d), was die prognostische Bedeutung des ICR-Wertes bei Darmkrebs bestätigt.
Abbildung 1. Studiendesign der AC-ICAM-Studie, immunbezogene Gensignatur, immunologische und molekulare Subtypen und Überleben.
ICR erfasst tumorreiche, klonal amplifizierte T-Zellen
Nur ein kleiner Teil der in Tumorgewebe infiltrierenden T-Zellen (weniger als 10 %) ist spezifisch für Tumorantigene. Daher werden die meisten intratumoralen T-Zellen als Bystander-T-Zellen bezeichnet. Die stärkste Korrelation mit der Anzahl konventioneller T-Zellen mit produktiven TCRs wurde in Stromazell- und Leukozyten-Subpopulationen (nachgewiesen durch RNA-Sequenzierung) beobachtet, die zur Abschätzung von T-Zell-Subpopulationen herangezogen werden können (Abbildung 2a). In den ICR-Clustern (gesamt und CMS-Klassifizierung) wurde die höchste Klonalität immunologischer SEQ-TCRs in den ICR-high- und CMS-Subtyp-CMS1/immune-Gruppen beobachtet (Abbildung 2c), die den höchsten Anteil an ICR-high-Tumoren aufwiesen. Unter Verwendung des gesamten Transkriptoms (18.270 Gene) zählten sechs ICR-Gene (IFNG, STAT1, IRF1, CCL5, GZMA und CXCL10) zu den zehn Genen mit der stärksten positiven Assoziation mit der TCR-ImmunoSEQ-Klonalität (Abbildung 2d). Die ImmunoSEQ-TCR-Klonalität korrelierte stärker mit den meisten ICR-Genen als die Korrelationen, die mit tumorresponsiven CD8+-Markern beobachtet wurden (Abbildung 2f und 2g). Zusammenfassend lässt die obige Analyse darauf schließen, dass die ICR-Signatur das Vorhandensein tumorangereicherter, klonal amplifizierter T-Zellen erfasst und deren prognostische Bedeutung erklären könnte.
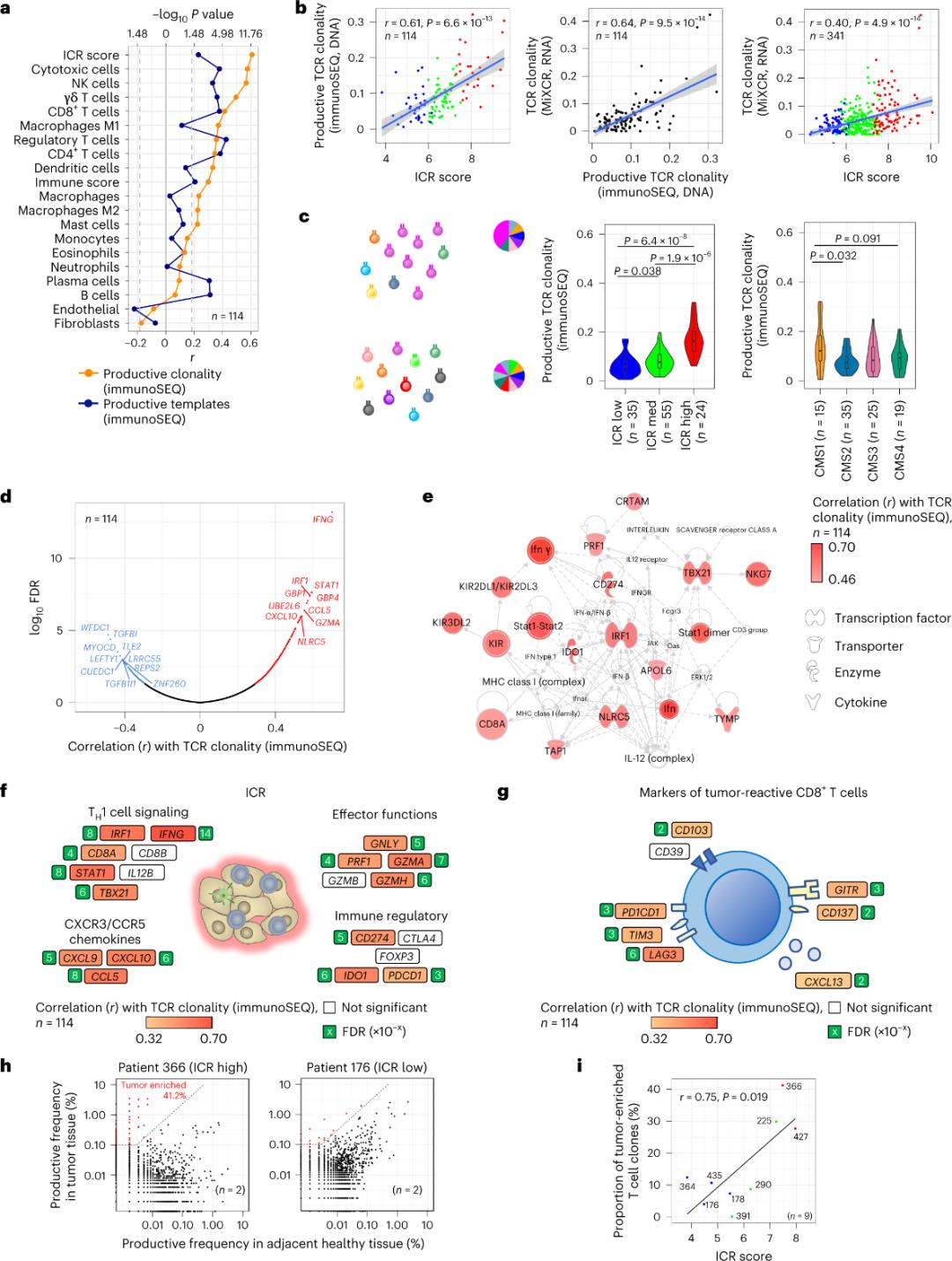
Abbildung 2. TCR-Metriken und Korrelation mit immunbezogenen Genen, immunologischen und molekularen Subtypen.
Zusammensetzung des Mikrobioms in gesundem Gewebe und Dickdarmkrebsgewebe
Die Forscher führten eine 16S-rRNA-Sequenzierung mit DNA durch, die aus jeweils korrespondierendem Tumor- und gesundem Kolongewebe von 246 Patienten extrahiert wurde (Abbildung 3a). Zur Validierung analysierten sie zusätzlich 16S-rRNA-Gensequenzierungsdaten von 42 weiteren Tumorproben, für die keine korrespondierende normale DNA zur Analyse verfügbar war. Zunächst verglichen die Forscher die relative Häufigkeit der Darmflora in den korrespondierenden Tumoren und dem gesunden Kolongewebe. Clostridium perfringens war in den Tumoren im Vergleich zu den gesunden Proben signifikant erhöht (Abbildung 3a–3d). Es zeigte sich kein signifikanter Unterschied in der Alpha-Diversität (Diversität und Häufigkeit der Arten in einer einzelnen Probe) zwischen Tumor- und gesunden Proben. In Tumoren mit hohem ICR-Wert wurde im Vergleich zu Tumoren mit niedrigem ICR-Wert eine geringfügige Reduktion der mikrobiellen Diversität beobachtet.
Um klinisch relevante Zusammenhänge zwischen mikrobiellen Profilen und klinischen Ergebnissen zu ermitteln, nutzten die Forscher 16S-rRNA-Gensequenzierungsdaten, um Mikrobiommerkmale zu identifizieren, die das Überleben vorhersagen. Auf der AC-ICAM246-Konferenz führten die Forscher ein OS-Cox-Regressionsmodell durch, das 41 Merkmale mit von Null verschiedenen Koeffizienten (die mit einem unterschiedlichen Mortalitätsrisiko assoziiert sind) auswählte, sogenannte MBR-Klassifikatoren (Abbildung 3f).
In dieser Trainingskohorte (ICAM246) war ein niedriger MBR-Wert (MBR < 0) mit einem signifikant geringeren Sterberisiko (85 %) assoziiert. Die Forscher bestätigten den Zusammenhang zwischen niedrigem MBR-Wert (Risiko) und verlängertem Gesamtüberleben in zwei unabhängig validierten Kohorten (ICAM42 und TCGA-COAD) (Abbildung 3). Die Studie zeigte eine starke Korrelation zwischen endogastrischen Kokken und MBR-Werten, die in Tumorgewebe und gesundem Kolongewebe vergleichbar waren.
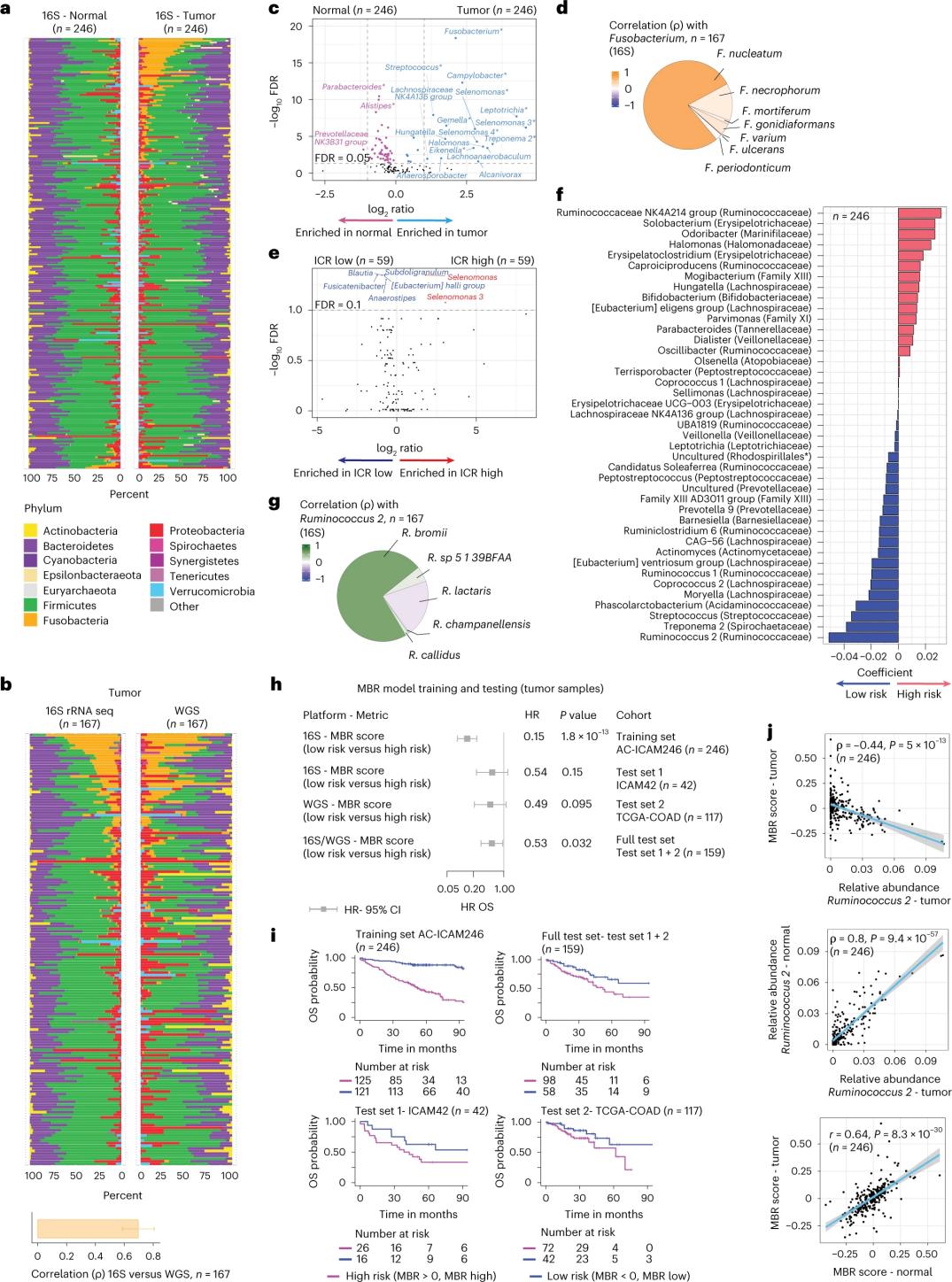
Abbildung 3. Mikrobiom in Tumorgewebe und gesundem Gewebe und der Zusammenhang mit ICR und Patientenüberleben.
Abschluss
Der in dieser Studie angewandte Multi-Omics-Ansatz ermöglicht die umfassende Erfassung und Analyse der molekularen Signatur der Immunantwort bei Darmkrebs und deckt die Interaktion zwischen Mikrobiom und Immunsystem auf. Die Sequenzierung des tiefen TCR-Gens von Tumor- und gesundem Gewebe ergab, dass die prognostische Bedeutung des ICR auf dessen Fähigkeit zurückzuführen sein könnte, tumorreiche und möglicherweise tumorspezifische T-Zellklone zu erfassen.
Durch die Analyse der Tumormikrobiomzusammensetzung mittels 16S-rRNA-Gensequenzierung in AC-ICAM-Proben identifizierte das Team eine Mikrobiomsignatur (MBR-Risikoscore) mit hoher prognostischer Aussagekraft. Obwohl diese Signatur aus Tumorgewebeproben abgeleitet wurde, zeigte sich eine starke Korrelation zwischen gesundem Kolorektum und dem Tumor-MBR-Risikoscore. Dies deutet darauf hin, dass diese Signatur die Zusammensetzung des Darmmikrobioms von Patienten widerspiegeln könnte. Durch die Kombination der ICR- und MBR-Scores konnte ein multi-omischer Biomarker identifiziert und validiert werden, der das Überleben von Patienten mit Darmkrebs vorhersagt. Der multi-omische Datensatz der Studie stellt eine wertvolle Ressource dar, um die Biologie von Darmkrebs besser zu verstehen und personalisierte Therapieansätze zu entwickeln.
Veröffentlichungsdatum: 15. Juni 2023
 中文网站
中文网站