Während der PCR-Reaktion treten häufig Störfaktoren auf.
Aufgrund der sehr hohen Sensitivität der PCR gilt Kontamination als einer der wichtigsten Faktoren, die das Ergebnis der PCR beeinflussen und zu falsch positiven Ergebnissen führen können.
Ebenso wichtig sind die verschiedenen Ursachen für falsch-negative Ergebnisse. Werden ein oder mehrere essentielle Bestandteile der PCR-Mischung oder die Amplifikationsreaktion selbst gehemmt oder gestört, kann dies den diagnostischen Test beeinträchtigen. Dies kann zu einer reduzierten Effizienz und sogar zu falsch-negativen Ergebnissen führen.
Neben der Hemmung kann es auch aufgrund von Transport- und/oder Lagerbedingungen vor der Probenvorbereitung zu einem Verlust der Integrität der Zielnukleinsäuren kommen. Insbesondere hohe Temperaturen oder unsachgemäße Lagerung können Zellen und Nukleinsäuren schädigen. Die Fixierung von Zellen und Gewebe sowie die Paraffineinbettung sind bekannte Ursachen für DNA-Fragmentierung und ein anhaltendes Problem (siehe Abbildungen 1 und 2). In diesen Fällen hilft selbst eine optimale Isolierung und Aufreinigung nicht.
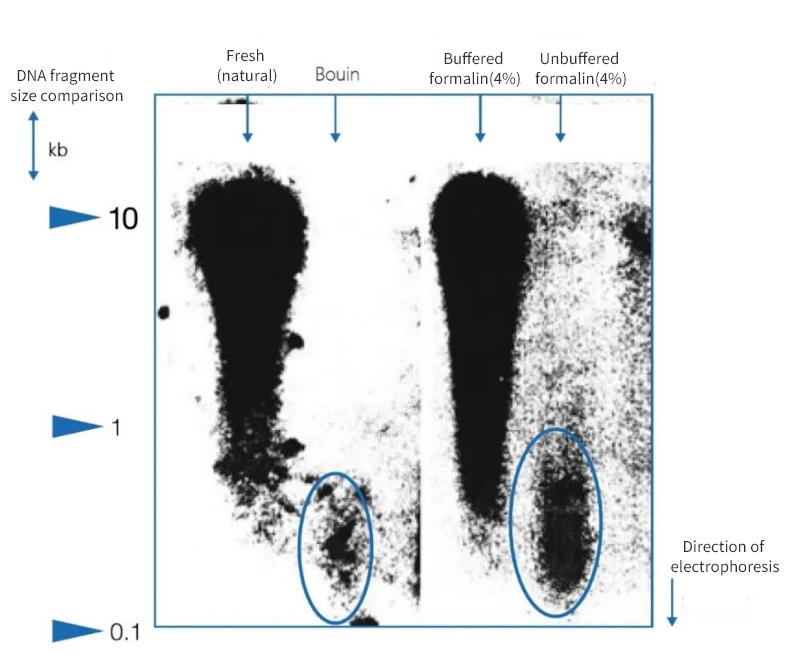
Abbildung 1 | Einfluss der Immobilisierung auf die DNA-Integrität
Die Agarose-Gelelektrophorese zeigte, dass die Qualität der aus Paraffinschnitten von Autopsien isolierten DNA erheblich variierte. Abhängig von der Fixierungsmethode enthielten die Extrakte DNA mit unterschiedlichen durchschnittlichen Fragmentlängen. DNA blieb nur erhalten, wenn sie in nativen, gefrorenen Proben oder in gepuffertem, neutralem Formalin fixiert wurde. Die Verwendung einer stark sauren Bouin-Fixierlösung oder von ungepuffertem, ameisensäurehaltigem Formalin führte zu einem signifikanten DNA-Verlust. Die verbleibende Fraktion ist stark fragmentiert.
Links wird die Länge der Fragmente in Kilobasenpaaren (kbp) angegeben.
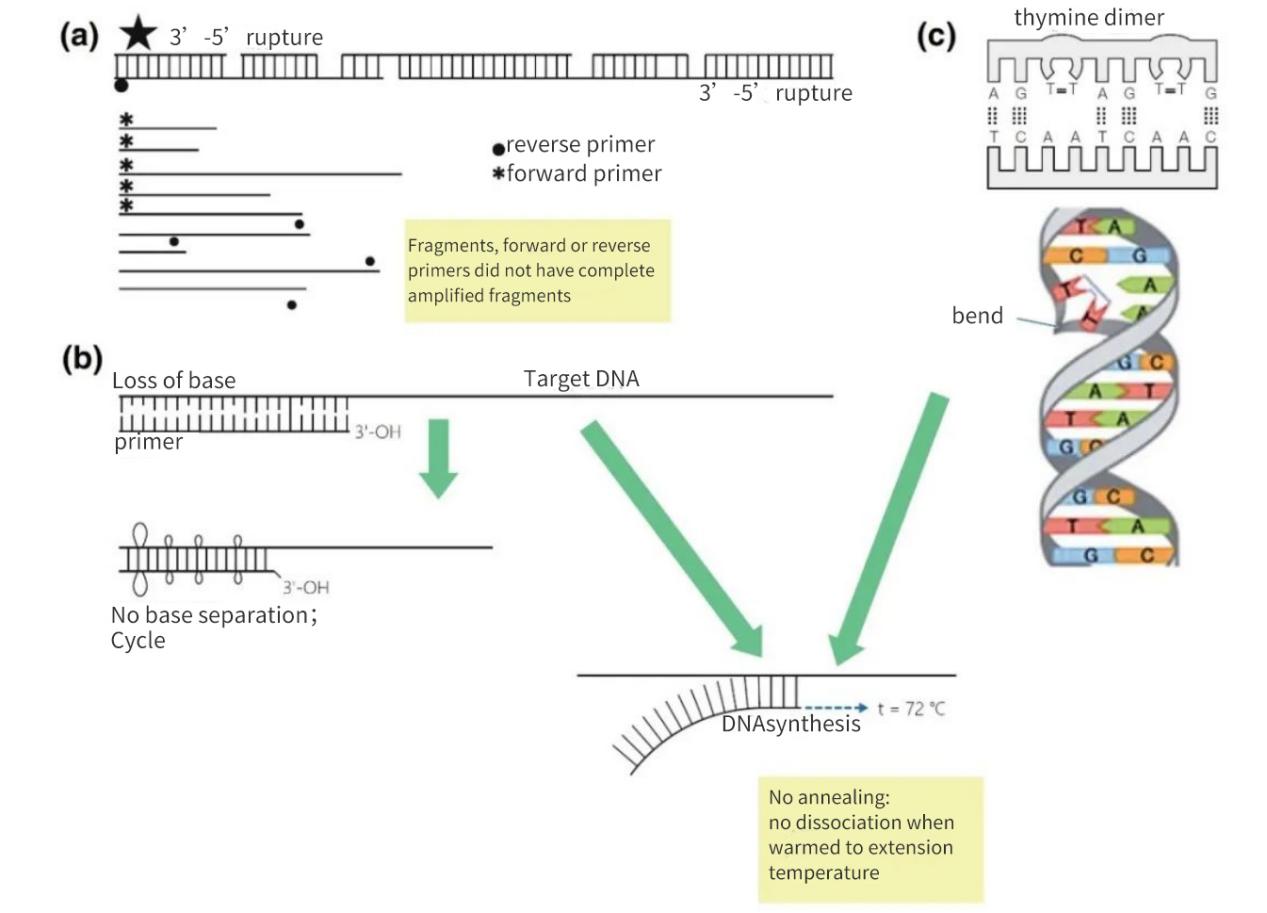
Abbildung 2 | Verlust der Integrität von Nukleinsäure-Targets
(a) Eine 3′-5′-Lücke auf beiden Strängen führt zu einem Bruch der Ziel-DNA. Die DNA-Synthese findet dennoch am kleinen Fragment statt. Fehlt jedoch eine Primerbindungsstelle auf dem DNA-Fragment, erfolgt lediglich eine lineare Amplifikation. Im günstigsten Fall können sich die Fragmente gegenseitig resättigen, die Ausbeuten sind jedoch gering und liegen unterhalb der Nachweisgrenze.
(b) Der Verlust von Basen, hauptsächlich aufgrund von Depurinierung und Thymidindimerbildung, führt zu einer Verringerung der Anzahl von Wasserstoffbrückenbindungen und einer Senkung der Schmelztemperatur (Tm). Während der verlängerten Erwärmungsphase lösen sich die Primer von der Matrix-DNA und hybridisieren selbst unter weniger strengen Bedingungen nicht mehr.
(c) Benachbarte Thyminbasen bilden ein TT-Dimer.
Ein weiteres häufiges Problem in der molekularen Diagnostik ist die suboptimale Freisetzung der Zielnukleinsäuren im Vergleich zur Phenol-Chloroform-Extraktion. In Extremfällen kann dies zu falsch-negativen Ergebnissen führen. Durch Kochlyse oder enzymatische Verdauung von Zelltrümmern lässt sich zwar viel Zeit sparen, jedoch führt diese Methode aufgrund der unzureichenden Nukleinsäurefreisetzung oft zu einer geringen PCR-Sensitivität.
Hemmung der Polymeraseaktivität während der Amplifikation
Im Allgemeinen dient der Begriff der Hemmung als Sammelbegriff für alle Faktoren, die zu suboptimalen PCR-Ergebnissen führen. Biochemisch betrachtet beschränkt sich die Hemmung auf die Aktivität des Enzyms, d. h. sie reduziert oder verhindert die Substrat-Produkt-Umwandlung durch Wechselwirkung mit dem aktiven Zentrum der DNA-Polymerase oder ihrem Cofaktor (z. B. Mg²⁺ bei der Taq-DNA-Polymerase).
Bestandteile der Probe oder verschiedene Puffer und Extrakte, die Reagenzien enthalten, können das Enzym direkt hemmen oder seine Cofaktoren (z. B. EDTA) binden, wodurch die Polymerase inaktiviert wird und es wiederum zu verminderten oder falsch negativen PCR-Ergebnissen kommt.
Viele Wechselwirkungen zwischen Reaktionskomponenten und zielmolekülhaltigen Nukleinsäuren werden jedoch auch als „PCR-Inhibitoren“ bezeichnet. Sobald die Zellintegrität durch die Isolierung gestört und die Nukleinsäure freigesetzt wird, können Wechselwirkungen zwischen der Probe und der umgebenden Lösung sowie der festen Phase auftreten. Beispielsweise können „Scavenger“ einzel- oder doppelsträngige DNA über nicht-kovalente Wechselwirkungen binden und die Isolierung und Aufreinigung beeinträchtigen, indem sie die Anzahl der Zielmoleküle, die schließlich das PCR-Reaktionsgefäß erreichen, reduzieren.
Im Allgemeinen sind PCR-Inhibitoren in den meisten Körperflüssigkeiten und Reagenzien, die für klinische Diagnosetests verwendet werden (Harnstoff im Urin, Hämoglobin und Heparin im Blut), in Nahrungsergänzungsmitteln (organische Komponenten, Glykogen, Fett, Ca2+-Ionen) und in Umweltkomponenten (Phenole, Schwermetalle) vorhanden.
| Inhibitoren | Quelle |
| Calciumionen | Milch, Knochengewebe |
| Kollagen | Gewebe |
| Gallensalze | Kot |
| Hämoglobin | Im Blut |
| Hämoglobin | Blutproben |
| Huminsäure | Boden, Pflanze |
| Blut | Blut |
| Lactoferrin | Blut |
| (Europäisches) Melanin | Haut, Haare |
| Myoglobin | Muskelgewebe |
| Polysaccharide | Pflanze, Kot |
| Protease | Milch |
| Harnstoff | Urin |
| Mukopolysaccharid | Knorpel, Schleimhäute |
| Lignin, Zellulose | Pflanzen |
Häufige PCR-Inhibitoren finden sich in Bakterien und eukaryotischen Zellen, nicht-zielgerichteter DNA, DNA-bindenden Makromolekülen von Gewebematrices sowie in Laborgeräten wie Handschuhen und Kunststoffen. Die Reinigung der Nukleinsäuren während oder nach der Extraktion ist die bevorzugte Methode zur Entfernung von PCR-Inhibitoren.
Heutzutage können diverse automatisierte Extraktionsgeräte viele manuelle Protokolle ersetzen, doch eine vollständige Ausbeute und/oder Reinigung der Zielmoleküle wurde bisher nicht erreicht. Potenzielle Inhibitoren können weiterhin in den gereinigten Nukleinsäuren vorhanden sein oder bereits ihre Wirkung entfaltet haben. Es gibt verschiedene Strategien, um die Wirkung von Inhibitoren zu reduzieren. Die Wahl der geeigneten Polymerase kann die Inhibitoraktivität maßgeblich beeinflussen. Weitere bewährte Methoden zur Reduzierung der PCR-Inhibition sind die Erhöhung der Polymerasekonzentration oder die Anwendung von Additiven wie BSA.
Die Hemmung von PCR-Reaktionen kann durch interne Prozessqualitätskontrolle (IPC) nachgewiesen werden.
Es ist wichtig, alle Reagenzien und sonstigen Lösungen des Extraktionskits, wie Ethanol, EDTA, CETAB, LiCl, GuSCN, SDS, Isopropanol und Phenol, durch gründliches Waschen aus dem Nukleinsäureisolat zu entfernen. Je nach Konzentration können diese die PCR aktivieren oder hemmen.
Veröffentlichungsdatum: 19. Mai 2023
 中文网站
中文网站